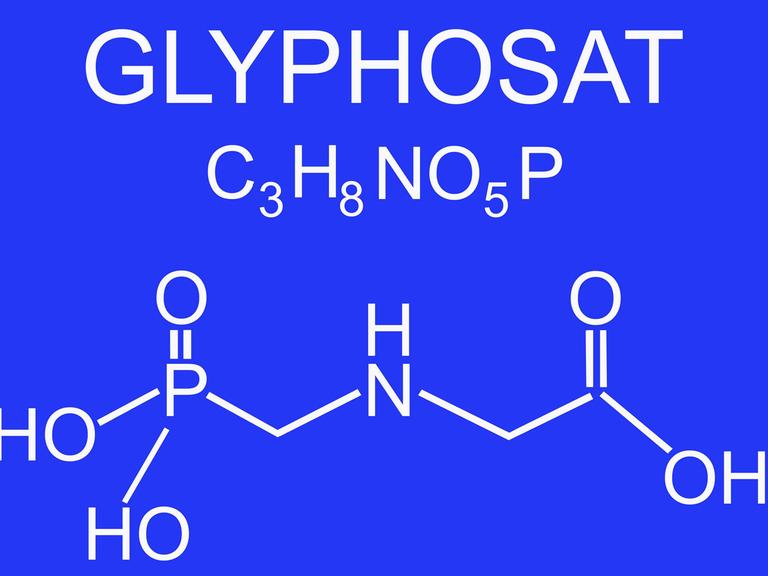
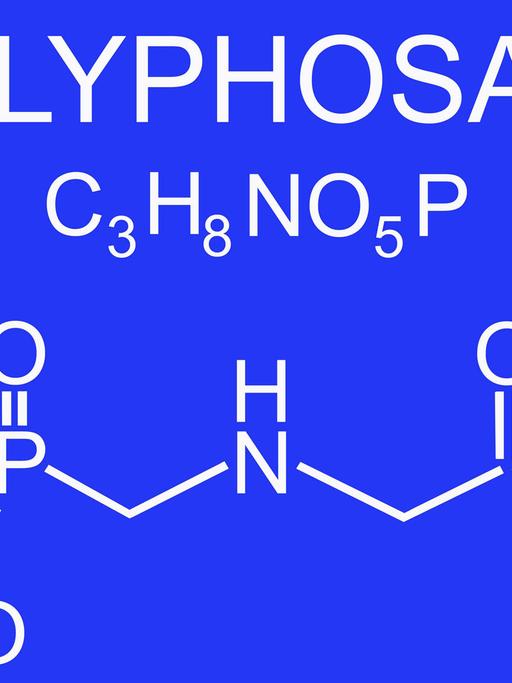
Genveränderung ist längst in unseren Mägen gelandet
Mit dem Verfahren namens CRISPR/Cas9 lassen sich Gene manipulieren. Die Technologie wird schon lange in der Lebensmittelindustrie genutzt - um etwa Bakterien zu schaffen, mit denen Joghurt, Salami oder Roggenbrot erzeugt wird. Juristisch können diese Lebensmittel nicht als "genverändert" deklariert werden, es fehlten die typischen Spuren.
Es erstaunt immer wieder, mit welchem Getöse Forschungsergebnisse ohne Erkenntnisgewinn als Weltneuheit unters Volk gebracht werden. Seltsamerweise finden echte Durchbrüche nicht immer die Resonanz, die ihnen gebührt. Ein solcher ist die CRISPR/Cas9-Technik. Das Verfahren ist so genial, dass viele Fachleute erwartet hatten, dass die beiden Forscherinnen mit dem Nobelpreis geehrt werden. Doch es sollte anders kommen und Jennifer Doudna und Emmanuelle Charpentier gingen leer aus.
Hinter dem kryptischen Namen CRISPR/Cas9 verbirgt sich ein elegantes Schreibprogramm. Damit lassen sich Gene geradeso wie Texte editieren. Man kann Abschnitte im Genom entfernen, verschieben, korrigieren oder auch neu schreiben. Und das mit bisher unerreichter Präzision, Effizienz und Flexibilität. Was früher ein Jahr intensiver Arbeit im Labor erforderte, gelingt damit in zwei Wochen. Das ist nur der Zwischenstand. Die Zeiträume werden sich noch erheblich verkürzen.
Das Verfahren verdanken wir der Entdeckung eines Krankheits-Gedächtnisses in – Bakterien. Krank werden Bakterien dann, wenn sie von Viren befallen werden – Viren, die Bazillen krank machen, heißen korrekt Phagen. Die Bakterien merken sich deren genetische Fingerabdrücke und speichern sie in ihrem Genom. Bei einem neuen Angriff durch einen Phagen gleichen sie dessen Fingerabdruck mit den abgespeicherten Daten ab. Ist der Erreger bekannt, dann synthetisiert die befallene Bakterie ein Enzym, das wie eine Schere das Erbgut des Phagen zerstört. Damit ja kein Fehler passiert, bekommt die Schere eine exakte Zielangabe mit auf den Weg, wo es das Erbgut des Virus zerschnippeln soll.
Wenn man das System ein wenig umprogrammiert, lassen sich damit im Labor Erbinformationen neu schreiben. Dem "Editieren von Genomen", schreibt die Fachpresse, "scheinen technologisch kaum noch Grenzen gesetzt." Das sei womöglich der Einstieg in einen Experimentierkasten für Schüler, mit dem sie sich ihr eigenes Haustier erschaffen könnten, so wird spekuliert. Denn nach einer kurzen Einweisung kann das Verfahren schon heute von Schülern praktiziert werden.
Retroviren nisten sich ins Erbgut von Lebewesen
Die erste erfolgreiche Anwendung galt noch einfachen Organismen, nämlich Bakterien, die als Starterkulturen zur Herstellung von Lebensmitteln benötigt werden. Wenn Phagen Starterkulturen befallen, dann misslingen Joghurt, Salami und Roggenbrot. Die Industrie benötigt phagenresistente Bakterien. Die bekommt sie nun schnell und nach Wunsch. Auch die Pflanzenzüchter frohlocken. Endlich ist es möglich, Nutzpflanzen mit einfachen Mitteln vor Viren zu schützen. Denn das was bei Bakterien möglich ist, funktioniert genauso bei Pflanzen. Beim Auftreten neuer Erreger spielt vor allem die Schnelligkeit eine Rolle, mit der es jetzt möglich ist, diese zu bekämpfen.
Bei Nutzvieh wird derzeit an einem ganz speziellen Fall gearbeitet, an den Retroviren. Retroviren sind Viren, die sich ins Erbgut eines Lebewesens einnisten können und von dort aus für ihre Verbreitung sorgen. Manche werden weitervererbt, andere werden wie bei einem Infekt weitergereicht. Bei Schweinen gelang es bereits, solche Retroviren aus dem Erbgut zu entfernen. Das bekannteste Retrovirus ist übrigens HIV, der Erreger von AIDS – aber auch einige Krebserkrankungen und Nervenleiden werden von Retroviren hervorgerufen. Klar, dass sich dafür die Pharmawirtschaft brennend interessiert.
Das Verfahren ist nicht nur einfach und präzise – es hinterlässt keine Spuren. Es gibt keine Markergene – nichts. Aufgrund des Fehlens charakteristischer Spuren fallen sie nicht einmal mehr unter die juristische Definition genveränderter Organismen. Forderungen, die neue Technik gesetzlich zu regeln oder zu kennzeichnen, sind damit sinnlos. Der Wunsch nach einem globalen Verbot ebenso. Aufhalten lässt sich die CRISPR/Cas9-Technik nicht. Ihre Ergebnisse sind längst in unseren Mägen gelandet. Eine Flut von Anwendungen in anderen Lebensbereichen wird folgen. Mahlzeit!
Literatur:
Charpentier E, Doudna JA: Biotechnology: Rewriting a genome. Nature 2013; 495: 50–51
Doudna JA, Charpentier E: The new frontier of genome engineering with CRISPR-Cas9. Science 2014; 346: 1077
Hsu PD et al: Development and applications of CRISPR-Cas9 for genome engineering. Cell 2014; 157: 1262-1278
Bortesi L, Fischer R: The CRISPR/Cas9 system for plant genome editing and beyond. Biotechnology Advances 2015; 33: 41-52
Zhang S: Cheap DNA sequencing is here, writing is next. Wired.com 20. Nov. 2015
Heller P: CRISPR/Cas9. Science-skeptical.de, Stand 15. Okt. 2015
Redaktion Pflanzenforschung.de: Was CRISPR/Cas leisten kann. Bundesministerium für Bildung und Forschung: Pflanzenforschung.de Journal 22. Okt. 2015
Dominguez AA et al: Beyond editing: repurposing CRISPR-Cas9 for precision genome regulation and interrogation. Nature Reviews. Molecular Cell Biology 2015; Epub ahead of print
Xie K, Yang Y: RNA-guided genome editing in plants using a CRISPR–Cas system. Molecular Plant 2013; 6: 1975–1983
Reardon S: Gene-editing record smashed in pigs. Nature DOI: 10.1038/nature.2015.18525
Lijuan Y et al: The application of CRISPR-Cas9 gene editing technology in viral infection diseases. Hereditas (Beijing) 2015; 37: 412-418