Sie rekonstruieren sozusagen Außen, Mitte und Innen vom Uterus und zeigen dann, welche Prozesse nötig sind, damit das gelingt, durch diese Schicht durchzukommen und eine Gefäßversorgung zu induzieren: Eine Veränderung großer Gefäße der Mutter, all die Prozesse, die der Embryo jetzt braucht, um eine Plazenta zu bilden.
Wir haben sehr viele Vorgänge bei der Einnistung, die wir nicht gut verstehen und bei denen wir aber wissen, dass sie Schwangerschaften verhindern. Da glaube ich, müssen wir die Mechanismen besser verstehen. Das kann man mit diesem System untersuchen. Wir müssten vielleicht, wenn wir das dann haben, Bedingungen herstellen, die bei pathologischen Fällen erklären können, warum die Einnistung nicht geht.
Forschung mit Uterusmodell
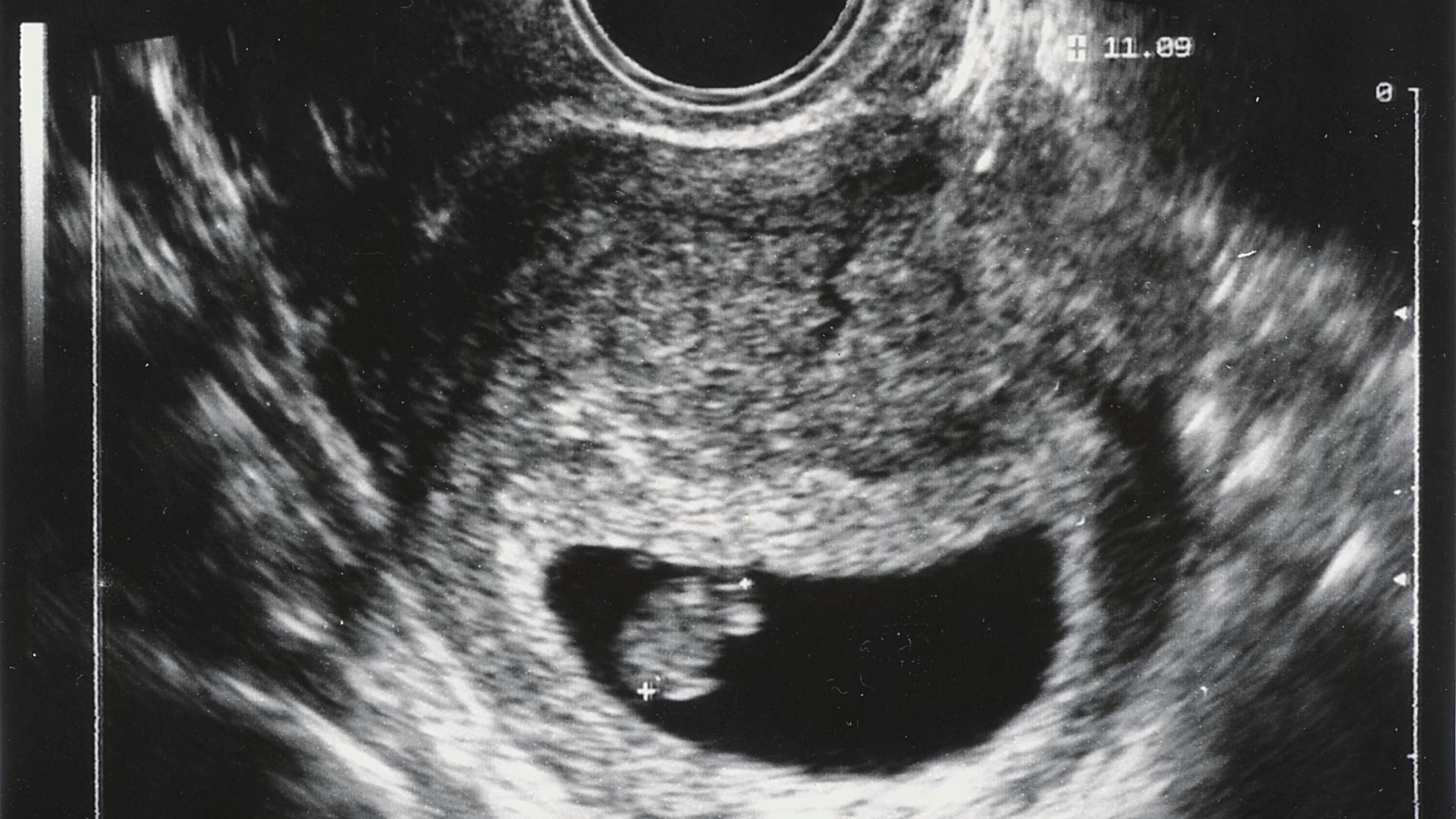
Ultraschallbild eines menschlichen Embryos: Mit einem Modell wollen Forschende einige Fragen zur ganz frühen Schwangerschaft klären. © Getty Images / Yiming Chen
Den Rätseln der Einnistung auf der Spur
06:19 Minuten

Was in den ersten Tagen einer Schwangerschaft passiert, ist für Medizinerinnen und Mediziner noch immer eine Art Blackbox. Sehr oft geht dabei etwas schief. Was genau, wollen Forschende nun an einem Modell der menschlichen Gebärmutter untersuchen.
Eine Schwangerschaft ist eine Gleichung mit vielen Unbekannten. Jeden Monat reift eine einzige der etwa 400.000 weiblichen Eizellen heran und wird - mit Glück - von einer Spermienzelle befruchtet. Doch viele dieser befruchtetet Eizellen bleiben im Eileiter hängen oder sie versuchen, sich schon dort einzunisten.
Beides führt zu Abgängen. Doch selbst wenn es die befruchtete Eizelle bis in die Gebärmutter schafft, stehen die Chancen auf Schwangerschaft weiterhin schlecht, sagt der Münsteraner Reproduktionsmediziner Stefan Schlatt.
„Eigentlich ist das ein Prozess, der sehr, sehr gefährlich ist. Wir sind nie wieder im Leben ein größeres Risiko eingegangen, als sich bei der Mutter einzunisten, denn eine zweidrittel Chance zu sterben - das würde nie einer riskieren“, erklärt er.
Konkret heißt das: zwei von drei befruchteten Eizellen gehen zugrunde, weil sie sich nicht erfolgreich in die Uterusschleimhaut einnisten können. „So gesehen ist es ein riesiger Verlust von Leben, der dort passiert, von dem wir aber nicht genau verstehen, welche Prozesse da gestört sind.“
„Wir spielen die Vorgänge nach“
Genau diese Wissenslücke wollen Monica Mainigi von der Universität von Pennsylvania und ihr Team nun schließen. Sie haben ein künstliches Organ entwickelt, das sie einerseits mit den Zellen des frühen Embryos bestücken können, andererseits mit den Zellen, aus denen sich die Gebärmutter und die dazugehörige Schleimhaut zusammensetzt.
„Es ist etwa so groß wie eine größere Münze und besteht aus einem synthetischen Material, in dem sich drei Kanäle befinden. Diese Kanäle können wir mit verschiedenen Zelltypen bestücken und dann beobachten, wie diese miteinander interagieren“, erklärt sie. „Wir spielen also die Vorgänge nach, wenn der Embryo im Uterus ankommt und sich in der Schleimhaut einnisten will.“
Dabei interessiert die Forschenden vor allem, welche Signale diese sehr frühe Form eines Embryos, Fachleute reden hier eigentlich von Blastozysten, aussenden.
Sie wollen herausfinden, wie sich wiederum die Zellen der Uterusschleimhaut in dieser frühen Einnistungsphase verhalten. „Also wie heftet sich der Embryo an die Schleimhaut an“, sagt Monica Mainigi. „Was passiert da genau? Welche Zellen sind daran beteiligt?“
Die Einnistung – ein sehr komplexer Prozess
Denn woher weiß der Embryo, an welcher Stelle er sich im Uterus einnisten soll? Wie baut er dann eine Verbindung zu den Blutgefäßen auf, die ihn mit Nährstoffen versorgen. Und wie verhindert er, dass die Immunzellen der Mutter ihn angreifen? Genau diese Rätsel kann die Forschung mit dem neuen Modell lösen, sagt Stefan Schlatt.
Allerdings haben die ersten Versuche gezeigt: Wie so oft ist das Zusammenspiel der Zellen im Körper extrem kompliziert.
Eine Art Fremdkörper, der sich andockt
„Unser wichtigstes Ergebnis ist bisher, dass einfach so viele verschiedene Zelltypen in dieser Einnistung involviert sind und eine Rolle spielen“, erzählt Monica Mainigi. „Besonders wichtig sind die Endothelzellen, also die Zellen, mit denen die Blutgefäße von innen ausgekleidet sind. Sie geben die Signale an die Zellen der Plazenta, die dann in die Schleimhaut einwachsen kann.“
Die Plazenta wird vom Embryo selbst gebildet: Ein kompliziertes Versorgungssystem, das sich direkt an den Blutkreislauf der Mutter anschließt. Über diese Kanäle zweigt der Embryo neun Monate wichtige Nährstoffe ab, aber auch Sauerstoff.
„Also eigentlich kann man sagen: Der Embryo ist für die Mutter in dem Moment ein Parasit. Ein Parasit, der durch eine lokale Entzündungsreaktion in dieser endometrialen Schleimhaut eine Reaktion auslöst, die er dann nutzt, um sich unter die Schleimhaut der Mutter zu bewegen“, erklärt Stefan Schlatt.
„Dann programmiert er eben, nachdem es ihm gelungen ist, durch diese Zellschicht durchzukommen, programmiert er eben eine ganze Menge um. Und das sind genau die Prozesse, die sie untersuchen.“
Normalerweise wehrt sich das Immunsystem, wenn ein Fremdkörper eindringt oder eine Entzündungsreaktion auslöst. Doch irgendwie schafft es der Embryo, diese körpereigene Abwehr zu besänftigen. Wie, auch das hoffen Monica Mainigi und ihr Team mithilfe ihres Modells besser verstehen zu können.
Komplikationen und Fehlgeburten verhindern
Denn klar ist: Viele Frauen können nicht schwanger werden, weil sich ihr Immunsystem gegen die befruchtete Eizelle wehrt.
Wir hoffen, mithilfe unseres Modells zu verstehen, was vor sich geht, wenn nicht alles glatt läuft. Wenn Frauen zum Beispiel häufiger Fehlgeburten haben oder andere Komplikationen bei der Schwangerschaft. Wir schauen uns ihre Zellen an und sobald wir wissen, welche Zellen Probleme bei der Einnistung verursachen, können wir versuchen, diese Komplikationen zu verhindern.
Denn der Vorteil des Modells ist: Die Forschenden können für jede Patientin einen eigenen Miniatur-Uterus entwickeln, den sie mit deren individuellen Zellen bestücken.
Das soll die Chance für Frauen, die bislang nicht schwanger werden, zukünftig erhöhen helfen. Und auch Medikamente lassen sich an diesem Modell testen. Damit werden langfristig Versuche an Tieren überflüssig.